| Objetivos da experiência: Esta experiencia laboratorial tem como finalidade principal determinar o rendimento num processo de aquecimento da água, através da medição de um período de tempo, e identificar alguns dos fatores dos quais este rendimento pode depender. · Como podemos aumentar o rendimento no aquecimento? Esta é uma questão que se pretende estudar melhor ao longo desta atividade, tendo o objetivo de poder respondê-la no final de toda a experiência, fundamentando-a. Com esta experiência laboratorial permite também aos alunos, um aprofundamento dos concelhos estudados e precisos à boa execução da atividade. Introdução Teórica: Para a realização desta atividade experimental é necessário dominar alguns conceitos relacionados com as transferências de energia, que nos ajudaram em todo o processo da experiência. . Termodinâmica: estuda as relações entre o trabalho e o calor, mais explicitamente, estuda e reflete sobre os métodos para a transformação e energia térmica em energia de movimento. Esta área de estudo tem patentes duas leis aplicáveis a quaisquer sistemas na natureza: 1º. Lei da termodinâmica: princípio da conservação da energia aplicada a sistemas termodinâmicos; 2º. Lei da termodinâmica: apresenta os limites estabelecidas pela natureza quando se transforma calor em trabalho; Trataremos agora a distinção entre o calor e energia interna: . Calor: é a nomenclatura atribuída à energia, sendo transferida de um sistema para outro, unicamente em virtude da diferença de temperaturas entre eles. O calor é uma das formas de se transferir energia de um sistema para outro, e expressa a quantidade de energia transferida através da fronteira comum aos sistemas. . Energia interna: é o conteúdo total em energia de um sistema termodinâmico. É normalmente comum que a energia interna e o calor sejam confundidos, mas é bom saber que os dois constituem-se por definições bem distintas, definições que implicam o facto de se poder dizer sem erro que um sistema qualquer possui energia interna e também o facto de jamais se poder dizer que um sistema possui calor. Podemos ainda observar que a transferência de energia poder ser feita através de 3 processos: . Transferência de energia como trabalho: a interação mecânica do sistema com a sua vizinhança, está associada à aplicação de forças no sistema, as quais podem realizar trabalho. . Transferência de energia como calor: a energia transferida, como calor, de um sistema que está a uma temperatura mais elevada para outro que está a uma temperara mais baixa, fica neste último sistema como energia interna. Um sistema, depois de “absorver” ou depois de “perder” energia como calor, encontrar-se-á com um valor diferente de energia interna. Nesta atividade, iremos necessitar de outros conceitos como: A potência exprime-se em W (watt) e é definida pela razão entre a energia transferida, em J (joule) e o Δt, expresso em segundos, durante o qual a transferência se realizou, concluímos que: ![]() O rendimento- ᶯ , segundo as leis da termodinâmica, este conceito que calcula a unidade que expressa o grau de aproveitamento de um determinado processo e as perdas que o referido processo suporta. Nas máquinas, o rendimento consiste na relação entre a energia que estas convertem em trabalho e a energia total que consomem para o efeito, sendo geralmente expresso em percentagem. Traduz-se pela forma: ![]() Temos que sempre em consideração, que nem toda a energia que é fornecida a um sistema, é totalmente utilizada pelo mesmo, parte dela é dissipada para o meio, e outra é aproveitada para as funções do próprio sistema. Após a definição das noções acima descritas, a realização da experiência deve ser feita tendo em conta a explicação anterior, sendo que será utilizada uma placa de aquecimento caracterizada por uma potência elétrica, para aquecer uma dada massa de água contida num gobelé. A energia fornecida à placa de aquecimento é calculada com recurso à potência elétrica da placa, indicada pelo fabricante, e ao tempo durante o qual a placa está a fornecer energia ao recipiente com água, tal que: ![]() A energia que é recebida pela água, sob a forma de calor, vai produzir um acréscimo de energia interna da água, não havendo mudança de estado físico. Assim, a variação de energia interna da água, ou seja, a energia útil, igual á energia recebida sob a forma de calor, vai ser diretamente proporcional á massa de água, m, e á variação da temperatura, Δ t, experimentada pela água. ![]() A letra Q diz respeito à energia recebida sob a forma de calor, que faz com que a temperatura da água aumente, e c é a capacidade calorífica especifica, ou capacidade térmica mássica da água. Protocolo Experimental: Materiais: * Fonte de alimentação/energia * Placa de aquecimento- P. Selecta; COMBIMAX; mod. 230A; Watt- 5000; Volt- 220 * Balança- ± 0,01g; Matter Toledo; AB204; Max. 310g; Min. 0,02g * Gobelé- 800ml; Germany * Termómetro- -10ºC até 150ºC; Hernandez * Agitador * Cronómetro * Suporte Universal: garra, nós, rolha de borracha * Pega de borracha Reagentes: * Água- 400g Procedimento Experimental: 1º. Encheu-se o gobelé com água; 2º. Mediu-se a massa de água; 3º. Registou-se a temperatura da água; 4º. Montou-se o suporte universal; 5º. Colocou-se em frente do suporte universal, a placa que aquecimento; 6º. Ligou-se a placa à fonte de eletricidade; 7º. Colocou-se o gobelé sob a placa; 8º. Pôs-se o termómetro dentro da água; 9º. Cronometrou-se o tempo de exposição da água ao calor, até esta ter uma temperatura de 90ºC; 10º. Registou-se o tempo obtido até aos 90º C da água; 11º. Procedeu-se aos devidos cálculos (presentes na interpretação de resultados e cálculos); 12º. Realizou-se a limpeza e arrumação do material utilizado e do laboratório; Interpretação de Resultados e Cálculos: ![]() n – rendimento Eu – energia útil Ef – Energia fornecida Eu = Q = m × c × ∆θ m = 400g c água = 4186 J/Kg -1 ˚C -1 = 4,186 J/g ˚C Δϴ = ϴf - ϴi = 90˚C - 18˚C = 72˚C Eu = 400 × 4,186 × 72 = 120556,8 J Q – Energia necessária para fazer variar Δϴ˚C a temperatura da água m – massa da água utilizada Δϴ - variação da temperatura pretendida c – capacidade térmica mássica Ef = P × ∆t P – potência Δt – intervalo de tempo durante o aquecimento da água P = 500 W Δt = 05”18”22 = 5 × 60 + 18 = 318s Ef = 500 × 318 = 159000J Rendimento: n = ![]() × 100 = 75,82188679… ≈ 75,82% × 100 = 75,82188679… ≈ 75,82% Discussão: Fazendo uma primeira análise ao cálculo do rendimento, podemos afirmar que a energia útil tem de ser sempre inferior à energia fornecida. O valor do rendimento que foi obtido pelo nosso grupo é de cerca de 75%, sendo que podemos avaliar este valor e, dizer que é plausível. Utilizámos uma placa de aquecimento de pequenas dimensões, por isso, a energia em forma de calor da placa, era mais aproveitada pelo gobelé que continha a água. Comparando o valor do rendimento do nosso grupo, com os valores obtidos pelos outros grupos da turma, sendo que foram mais baixos que o nosso, cerca de 25%, e utilizaram placas de aquecimento de grandes dimensões, podemos afirmar que tendo uma placa de aquecimento de tamanho pequeno, é possível obter um maior valor de rendimento, visto que é aproveitada também uma maior quantidade de calor vindo da placa. Com uma placa de dimensão maior, mais energia, calor, é dissipado e desperdiçado para o meio, não sendo usufruído pela água. Conclusão: Na realização desta atividade não encontrámos qualquer dificuldade, visto que cumprimos os nossos objetivos definidos inicialmente. Conseguimos obter conclusões acerca desta atividade. A principal e mais importante, e que responde também à questão colocada nos objetivos acima. Podemos aumentar o rendimento no aquecimento utilizando materiais que sejam bons isoladores de calor; é conveniente que o recipiente deva estar tapado para evitar perdas de calor devido à evaporação da água; um dos fatores que ajuda também no aumento do rendimento no aquecimento é utilizando, nesse caso, uma placa de aquecimento de pequena dimensão, o que irá permitir uma quantidade inferior de calor emanado da placa, seja dissipado para o meio envolvente, sendo assim aproveitado a máxima energia calorífera possível. Contrariamente, se for utilizada uma placa de tamanho maior que o recipiente, em que se situa o que desejamos aquecer, o calor não será ao máximo aproveitado pelo sistema, havendo perdas significativas, existindo assim um menor valor de rendimento. 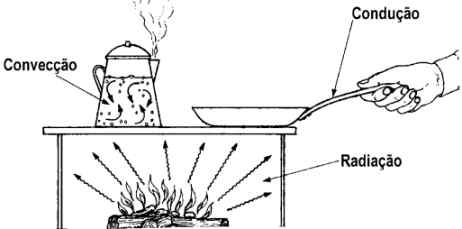 Anexo 1- transferência de energia como calor. 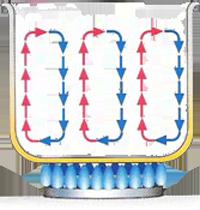 Anexo 2- Correntes de convecção de calor (azul corrente fria; vermelha corrente quente). 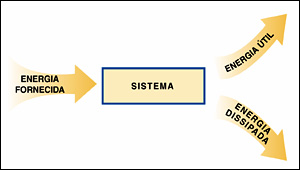 Anexo 3- energia fornecida a um sistema.  Anexo 4- suporte universal e balança  Anexo 5- experiência iniciada. Aquecimento da placa que produzirá calor ao gobelé que contém a água, e o termómetro para observarmos a temperatura da água até aos 90˚C, cronometrando o tempo. __________________________________ Outros Trabalhos Relacionados | | Ainda não existem outros trabalhos relacionados | |