|
Relatório de actividade
experimental
Métodos físicos de
separação de misturas
Objectivo
Separar, através de
processos físicos, os componentes de misturas homogéneas e heterogéneas.
Introdução Teórica
A matéria, de modo geral,
é encontrada na natureza na forma de misturas, conjunto de várias
substâncias. Estas misturas podem ter aparência, a olho nu, uniforme,
denominamo-las como homogéneas e quando estas nos apresentam uma forma
irregular, sem carácter homogéneo ou disformes denominamo-las por
heterogéneas.
Para realizarmos a
separação de misturas homogéneas podemos utilizar os seguintes
processos:
- Cristalização:
Utilizamos este processo quando queremos separar um componente sólido de
uma solução líquido-sólida. Podemos deixar evaporar o líquido até que a
solução fique saturada, a partir desse momento, o sólido vai-se separar
em cristais, mas para acelerar este processo aumentamos a temperatura e
o contacto com o ar. Os cristais húmidos podem ser secos com um papel de
filtro ou numa estufa, ou por filtração ou decantação, quando a
quantidade de líquido for muito grande.

Ilustração 1 -
Cristalização
- Destilação
fraccionada: Este processo utiliza-se quando os componentes a
separar são ambos voláteis, com pontos de ebulição próximos. Para a
separação dos componentes das misturas homogéneas líquido-líquido,
recorre-se muitas vezes à destilação fraccionada. Ao aquecer a mistura
num balão de destilação, os líquidos destilam-se na ordem crescente de
seus pontos de ebulição e podem ser separados.
- Destilação simples:
Utilizamos este processo quando a substância a separar é o único
componente volátil, com baixo ponto de ebulição, e quando os componentes
a separar têm pontos de ebulição muito diferentes. A destilação é eficaz
na separação de dois ou mais líquidos solúveis entre si. Cada líquido
possui uma temperatura de ebulição própria, e os líquidos podem ser
separados por meio de um destilador. Ferve-se uma solução formada por
líquidos num destilador, sendo a primeira fracção de líquido que se
recolhe a que corresponde ao líquido mais volátil, dado que foi o
primeiro a entrar em ebulição. Pode utilizar-se eficazmente sempre que
os líquidos misturados ou dissolvidos não possuem temperaturas de
ebulição muito parecidas. Em caso contrário é preciso utilizar
destilações muito mais complexas.

Ilustração 2 -
Destilação simples
Quando falamos em misturas
heterogéneas os processos que podemos utilizar na separação de misturas
são os seguintes:
- Separação
magnética: Trata-se de um método de separação específico das
misturas com um componente ferro magnético como o cobalto, o
níquel e, principalmente, o ferro. Estes materiais são extraídos pelos
ímanes, fenómeno que se pode aplicar para reter as suas partículas ou
para desviar a sua queda.
- Separação por
sublimação: A sublimação é a passagem directa de sólido para o
estado gasoso, sendo que algumas substâncias como o iodo sofrem
alterações, em determinadas condições de pressão e temperatura. A
sublimação pode-se aplicar às soluções sólidas e às misturas, sempre uma
das substâncias possa sofrer este fenómeno. Basta aquecer a mistura ou
solução à temperatura adequada e recolher os vapores que, quando
arrefecem, se vêem submetidos a uma sublimação regressiva, ou seja,
passam directamente de gás a sólido.
- Filtração:
Quando uma suspensão passa através de um papel de filtro, as suas
partículas ficam retidas se o diâmetro da malha que forma o papel for
suficientemente pequeno. No caso das partículas sólidas serem muito
pequenas pode recorrer-se a um filtro de porcelana porosa. O mais
corrente é o filtro de papel, que se dobra em quatro partes, formando-se
um cone que se adapta à forma do funil. Existem também filtro de areia,
argila e carvão.
- Decantação:
Trata-se da
separação de dois líquidos ou de um líquido e de um sólido (como o caso
indicado na ilustração 3), aproveitando a sua diferença de densidade.
Para separar um líquido de um sólido de maior densidade deixa-se a
repousar durante um certo tempo, para que este se deposite no fundo do
recipiente. Se as partículas sólidas forem muito pequenas, esse tempo
pode prolongar-se por horas ou até mesmo dias. A partir do momento em
que se depositou totalmente, inclina-se o recipiente com cuidado até se
verter o líquido sem que o sólido seja arrastado, para maior facilidade
desta tarefa utiliza-se uma vareta de vidro. A decantação é muito
utilizada para separar líquidos imiscíveis, ou seja, líquidos que não se
misturam. Para isso, coloca-se a mistura a ser separada num funil de
separação ou num funil de decantação. Quando a superfície de separação
das camadas líquidas estiver bem nítida, abre-se a torneira e deixa-se
escoar o líquido da camada inferior.
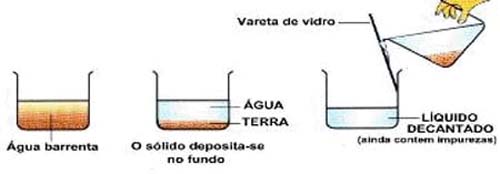
Ilustração 3 -
Decantação
- Centrifugação:
Quando numa mistura de sólidos e líquidos, os sólidos possuem uma
dimensão muito pequena, não é fiável proceder a uma filtração nem uma
decantação. O tamanho reduzido das partículas sólidas provoca uma
obstrução do filtro, tornando-a muito lenta mesmo que se produza vácuo
no interior do recipiente, para acelerar a filtração. Por outro lado, a
pequena dimensão das partículas faz com que sejam retidas pelo líquido,
de modo que podem demorar muito tempo a depositar-se no fundo do
recipiente, tornando ineficaz a decantação. Neste caso, introduz-se a
mistura em tubos de ensaio que, colocados numa centrifugadora, giram em
posição quase horizontal a grande velocidade, aumentando assim a rapidez
com que se deposita o sólido compactado no fundo do tubo. Verte-se o
líquido que fica sobre os resíduos do fundo do tubo de ensaio e fica
assim completa a separação.
Procedimentos
Para esta actividade
laboratorial, a sua preparação, consistiu na pesquisa dos processos
físicos de separação de misturas. No meu grupo de trabalho, a mistura
atribuída, foi, uma mistura heterogénea, de sal e areia.
Começámos primeiramente
por identificar os métodos a utilizar na separação de ambas as
substâncias. Concluímos então que para a realização desta separação
iríamos necessitar de dissolver o sal em água, de seguida faríamos uma
decantação ao mesmo tempo que filtraríamos a água devido às impurezas
depositadas da areia que se verificaram, posteriormente, na água, e por
fim teríamos de fazer uma vaporização da água salgada, filtrada, para
obtermos apenas os cristais de sal.
Reunido todo o material
necessário, principiámos a nossa actividade dissolvendo o sal, da
mistura, em água, num gobelé, e, completa a dissolução deixámos assentar
as partículas de areia e a maioria dos resíduos pertencentes á areia no
fundo do gobelé.
De seguida procedemos á
decantação que fizemos a par com a filtração da água salgada devido á
presença de impurezas provenientes da areia. A decantação foi feita com
o auxílio de uma vareta de vidro que colocamos apoiada ao interior do
papel de filtro dentro do funil de vidro, seguro pelo suporte universal
com a respectiva garra do mesmo, por onde vertemos a água salgada,
faseadamente, tentando ao máximo, não verter, juntamente com a água
salgada, a areia depositada no fundo do gobelé. O restante da
decantação, o gobelé com a areia molhada, foi colocado numa estufa
eléctrica, para assim se proceder á secagem da areia.
A água salgada ao ter sido
decantada para o funil foi imediatamente filtrada pelo papel de filtro
e, aos poucos, esse produto da filtração foi escorrendo para um copo de
precipitação maior que o primeiro utilizado.
Para finalizar a nossa
separação, colocámos o gobelé com a água filtrada sobre uma placa de
aquecimento e assim deu-se a vaporização da água, ficando no copo
resíduos de sal. Através deste procedimento separámos as duas
substâncias da mistura inicial. Concluímos a nossa actividade
experimental após a limpeza do material utilizado e respectiva
arrumação, bem como a limpeza da bancada de trabalho.
Material/Reagentes
Para a realização desta
actividade experimental utilizámos o seguinte material:
. Um gobelé de 100ml ± 5ml
. Um gobelé de 250ml ±
12,5ml
. Uma vareta de vidro
. Um esguicho
. Uma rede de amianto
. Uma placa de aquecimento
. Um funil de vidro
. Um suporte universal
. Papel de filtro
. Uma tenaz
Resultados/Registos/Observações
No decorrer da desta
actividade, logo após a dissolução do sal, observámos que a água, devido
á presença da areia, ficou com impurezas e logo após a filtração, estas
mesmas impurezas ficaram, quase na sua totalidade, retidas no papel de
filtro, embutido no funil de vidro.
Já no final da nossa
experiencia observámos que na vaporização, os cristais que se formaram
deveriam ser pequenos, comparando a vaporização ao processo de
cristalização, e o resultado que obtivemos foram uns resíduos de sal,
secos, dispostos de uma forma homogeneizada.
Observámos ainda o
resultado que obtivemos do gobelé que introduzimos na estufa.
Visualizámos uma camada com cerca de 3 mm de altura de cristais de sal,
que estava agregada às paredes do gobelé e uma camada super fina destes
mesmos cristais sobre a areia, já seca, no fundo do gobelé.
Contudo penso que para uma
separação eficaz e totalmente completa, os cristais de sal, que refiro
após o tempo de estufa do gobelé com areia, deveriam ser peneirados para
que ficasse assim totalmente separada a mistura.
Conclusão
Com esta actividade
experimental concluímos que em certos casos de misturas um só processo
de separação substâncias é ineficaz. Nesta actividade, tivemos de
recorrer a 3 métodos de separação de misturas até obtermos o resultado
final pretendido, o sal e a areia em separado.
Concluímos também que
todos os processos que efectuámos nos diversos métodos de separação
foram bem executados, não verificámos assim qualquer falha nesta
actividade experimental.
Bibliografia
Química em Contexto 10,
pág. 26-29 - Processos de destilação simples e fraccionada e filtração.
http://www.notapositiva.com/trab_estudantes/trab_estudantes/fisico_quimica/
fisico_quimica_trabalhos/processosseparmisturas.htm - Processos de
cristalização, centrifugação, decantação, separação por sublimação e
separação magnética.
http://www.prof2000.pt/users/anitsirc/cristaliza%C3%A7%C3%A3o.gif&imgrefurl=
http://www.prof2000.pt/users/anitsirc/corpomisturashomogeneas.htm -
Ilustração 1, 2 e 3.
Outros Trabalhos Relacionados
|
|
Ainda não existem outros trabalhos relacionados |
|