
O teu país
Lorem ipsum dolor sit amet, consectetur adipiscing elit, sed do eiusmod

Lorem ipsum dolor sit amet, consectetur adipiscing elit, sed do eiusmod
Todos os trabalhos publicados foram gentilmente enviados por estudantes – se também quiseres contribuir para apoiar o nosso portal faz como o(a) Rita Lorenço e envia também os teus trabalhos, resumos e apontamentos para o nosso mail: geral@notapositiva.com.
Trabalho (relatório) cujo objectivo foi a produção de biodiesel a partir de óleo vegetal usado, realizado no âmbito da disciplina de Química (12º ano).
Esta actividade experimental teve como objectivo a produção de biodiesel a partir de óleo vegetal usado.
Os óleos, apesar de serem considerados resíduos não perigosos, quando lançados nas redes de drenagem de águas residuais obstruem os filtros de gorduras existentes na ETAR, sendo um obstáculo ao seu bom funcionamento.
Assim, estes óleos podem ser utilizados para o fabrico de um combustível não poluente. Começa-se por filtrar o óleo usado, seguido da adição de uma mistura de metanol e hidróxido de sódio puro.
No final da experiência, o biodiesel é misturado com gasóleo, servindo como combustível.
Não se sabe ao certo quanto tempo durarão ainda as reservas de petróleo, gás natural ou carvão. É certo, contudo, que um dia os combustíveis fósseis se vão esgotar. Actualmente, estes são responsáveis por mais de 80% da energia produzida a nível global.
O petróleo é o que, ao ritmo do consumo actual, se esgotará mais cedo, pois, além de ser consumido como combustível ou carburante, é também uma matéria-prima essencial e insubstituível na indústria petroquímica.
É, portanto, imperativo saber racionalizar a utilização das reservas ainda existentes, poupando energia e aumentando a eficiência energética.
É do conhecimento geral que a problemática do petróleo não se limita à sua escassez como recurso. Existem também numerosos riscos ambientais associados não só à queima dos produtos petrolíferos - nomeadamente a poluição atmosférica, causada pela emissão de gases como o dióxido de carbono ou óxidos de enxofre e azoto, o efeito de estufa e consequentes alterações climáticas - mas também ao seu armazenamento e transporte.

Fig.1 – Plantação de colza
A comunidade internacional já se apercebeu disso e têm sido desenvolvidas alternativas para substituir o petróleo por “combustíveis limpos”, nomeadamente o biodiesel.
O biodiesel, ou éster etílico, é um combustível biodegradável que é fabricado a partir de fontes renováveis, como óleos vegetais, provenientes de girassol, colza, amendoim, etc.
Os óleos são gorduras líquidas, pertencentes a uma família da química orgânica, conhecida por lípidos. Os lípidos são substâncias insolúveis em água, que se podem extrair a partir de solventes orgânicos de baixa polaridade.
Quimicamente, as gorduras são ésteres carboxílicos derivados de um único álcool, o glicerol (propanotriol), e de um ácido gordo. O glicerol é um triálcool, sendo que as gorduras também são conhecidas por glicéridos, mais precisamente por triglicéridos.
Os ácidos gordos, por sua vez, provêm de gorduras naturais e são ácidos carboxílicos de cadeias carbonadas longas e não ramificadas, sendo que estas podem ser saturadas ou insaturadas.

Fig.2 – Formação de gordura
O biodiesel é um diéster, ou seja, é um glicérido com duas funções éster, proveniente de um ácido gordo, e como já foi referido, é um biocombustível líquido sintético renovável e biodegradável que se obtém a partir de lípidos naturais, como óleos vegetais ou gorduras animais, novos ou usados, mediante processo de transesterificação.
A transesterificação consiste na cisão de um éster, quando reage com um álcool, em geral, o metanol, na presença de um catalisador. O catalisador pode ser ácido ou alcalino, mas, em geral, utiliza-se o hidróxido de sódio ou de potássio. Como produtos de reacção obtêm-se: éster metílico do ácido gordo - o biodiesel -, e o glicerol, que é um subproduto.
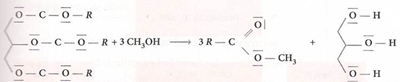
Fig.3 – Reacção de transesterificação
O biodiesel apresenta numerosas vantagens em relação aos restantes combustíveis, não só a nível ambiental, mas também no que respeita à aplicabilidade. O biodiesel pode misturar-se com o gasóleo, visto que as suas propriedades são idênticas.
A mistura deve conter 5% de diéster, mas pode ir até aos 30% para motores ~
“pesados”. O uso do biodiesel confere melhores características de lubricidade, aumentando o tempo de vida útil do motor.
Mundialmente, adoptou-se uma nomenclatura para identificar a concentração do biodiesel na mistura: biodiesel BDXX, onde XX é a percentagem em volume do biodiesel na mistura. Por exemplo, o BD2, BD5, BD20 e BD100 são combustíveis com uma concentração de 2%, 5%, 20% e 100% de biodiesel, respectivamente.
Apesar de existir BD100, as misturas em proporções volumétricas entre 5% e 20% são as mais usuais, sendo que para a mistura B5, não é necessária nenhuma adaptação dos motores.
Para além das vantagens já referidas, o biodiesel é menos poluente que o gasóleo, visto que é constituído por carbono neutro, sendo que as plantas capturam todo o CO2 emitido pela queima do biodiesel e não liberta compostos sulfurados e aromáticos para a atmosfera. Apresenta fácil transporte e armazenamento, visto que tem um baixo risco de explosão
– é necessária uma fonte de calor acima de 150ºC para explodir. Na queima, ocorre a combustão completa e o calor produzido por litro é quase igual ao do diesel, não havendo, portanto, perdas consideráveis de rendimento.

Fig.4 – Ciclo do biodiesel
Por último, a sua utilização pode ser um incentivo para a agricultura, contribuindo para a valorização económica dos terrenos abandonados.
Apesar de ser um combustível renovável, a sua capacidade de produção está limitada a áreas agrícolas disponíveis, que também terão de ser usadas para fins alimentares, sendo baixa a sua rentabilidade de produção: a substituição de 5% do gasóleo consumido em Portugal, com a actual produtividade da cultura do girassol, requereria a plantação de cerca de 500 000 hectares.
As baixas produções não permitem a construção de grandes unidades de processamento e levam a um custo do óleo que só dificilmente é compatível com o preço do gasóleo, junto do consumidor final. Para além disso, o uso de BD100 pode requerer a modificação de componentes do sistema do motor.
Outro potencial inconveniente derivado do uso de biodiesel é o aumento das emissões de compostos azotados. No entanto, este aumento não é muito significativo, tendo em conta as reduções significativas nas emissões dos restantes compostos.
Pelo exposto poder-se-á dizer que o biodiesel só parcialmente poderá substituir o gasóleo.
Material de laboratório:
1) Filtrou-se o óleo usado, com um pano, para eliminar os resíduos sólidos[1];[2];[3];
2) Colocaram-se 200mL desse óleo, num copo de precipitação[4];
3) Pesaram-se 1,31g de hidróxido de sódio, num vidro de relógio[5];
4) Mediram-se 50mL de metanol, com uma proveta[6];
NOTA: O metanol é uma substancia muito tóxica. Pode ser absorvido pela pele e se atingir os olhos pode provocar cegueira. Também há que ter cuidados muito especiais no manuseamento da solução alcalina pois é altamente corrosiva.
5) Passou-se o metanol para um copo de precipitação, ao qual se adicionou hidróxido de sódio[7];
NOTA: Este passo realizou-se na hotte, de modo a que os gases tóxicos libertados não fossem inalados.
6) Mexeu-se até o hidróxido de sódio se dissolver formação do metóxido de sódio (catalisador)[8];[9];
b Para facilitar e acelerar a dissolução, colocou-se a solução num balão volumétrico e agitou-se[10].
7) Aqueceu-se o óleo usado, entre os 50ºC e 60ºC, com ajuda de uma placa de aquecimento[11];
8) Juntou-se o metóxido obtido ao óleo e mexeu-se durante aproximadamente uma hora, tentando manter a solução sempre entre os 50/60⁰C[12];[13];[14];
9) Deixou-se repousar a solução até ser possível observar 2 fases[15]:
10) Mediram-se 20mL de biodiesel, numa proveta[16];
11) Juntaram-se 80mL de gasóleo ao biodiesel medido, de modo a obter o BD20[17];[18];
12) Lavou-se e arrumou-se todo o material utilizado.

A produção de biodiesel não levanta, a nível laboratorial, problemas de maior, se forem tidas em conta as regras de segurança adequadas aos reagentes utilizados.
A sua produção em larga escala poderá contudo ter que enfrentar questões de natureza não científica, nomeadamente associadas aos interesses dos lobbies petrolíferos, produção agrícola,…
A utilização do biodiesel em larga escala apresentaria, contudo, vantagens, tanto ao nível socioeconómico como também ambiental, face aos combustíveis tradicionais. Além de ser uma energia renovável também tem como consequência a diminuição dos gases com efeito de estufa.
Dado que não só as práticas de produção da matéria-prima se encontram bem disseminadas, como também as tecnologias de produção de biodiesel se encontram já disponíveis em algumas unidades industriais, acreditamos que a curto prazo o “diesel será verde”.
Livros:
Internet:





